infolinia: +48 800 174 902
Choroba Alzheimera

Choroba Alzheimera:
- jest najczęstszą postacią demencji (otępienia) i powoduje 60-70% jej przypadków,
- charakteryzuje się postępującym spadkiem funkcji poznawczych, stopniową utratą pamięci, zaburzeniami mowy, orientacji i zdolności uczenia się,
- objawia się głównie u osób, które ukończyły 65. rok życia, dlatego pierwsze objawy choroby Alzheimera są często mylone z naturalnym obniżaniem się sprawności umysłowej wraz z wiekiem, na chwilę obecną jest nieuleczalna - możemy jedynie spowolnić postęp choroby
W przypadku choroby Alzheimera, utrata funkcji poznawczych zachodzi zawsze znacznie szybciej niż u zdrowej starszej osoby, ze względu na postępujące zmiany w mózgu.
Etapy choroby Alzheimera
Zmiany w zachowaniu Twojego podopiecznego wywołane chorobą prawdopodobnie będą następowały stopniowo. Tempo, a także rodzaj zmian jest sprawą bardzo indywidualną.
-
1-2 rok. Otępienie łagodne
Wczesny etap jest często niezauważany, traktowany jako naturalne zmiany na skutek starzenia. Zmiany zachodzą stopniowo, a nasilenie objawów może być inne u różnych osób.
- zapominanie rzeczy, które się właśnie wydarzyły
- lekka utrata orientacji czasowej, w tym pory dnia, miesiąca, roku
- poczucie zagubienia w znanych miejscach
- lekkie trudności z komunikacją, jak trudności ze znalezieniem słów
- trudności z podejmowaniem decyzji i zarządzaniem finansami osobistymi
- trudności z wykonywaniem skomplikowanych zadań domowych
- zmiany zachowania: zmniejszenie aktywności i motywacji, utrata zainteresowań
- zmiany nastroju: depresja lub lęk, większa nerwowość
-
2-5 rok. Otępienie o średnim nasileniu
Na tym etapie wyraźnie zauważalne są nietypowe zachowania i pojawiają się widoczne ograniczenia.
- bardzo częste zapominanie rzeczy, które się niedawno wydarzyły, a także osób
- znaczna utrata orientacji czasowej, w tym pory dnia, miesiąca, roku
- gubienie się w znanych miejscach, w tym w domu
- rosnące trudności z komunikacją - z mową i zrozumieniem
- konieczność pomocy w codziennych czynnościach
- utrata zdolności przygotowywania posiłków, gotowania, robienia zakupów
- zmiany zachowania: niewytłumaczalne wędrówki, powtarzanie pytań, zaburzenia snu, omamy i urojenia
- zmiany nastroju: zachowania agresywne, brak samokontroli
-
5 rok i kolejne. Otępienie zaawansowane
Jest to etap prawie całkowitej zależności od opiekuna. Zakłócenia pamięci są bardzo poważne i występują liczne fizyczne ograniczenia.
- brak świadomości czasu i miejsca
- trudności ze zrozumieniem tego, co dzieje się wokół
- niemożność rozpoznania krewnych, znajomych, siebie, znanych przedmiotów
- konieczność karmienia
- trudności w połykaniu
- konieczność pomocy w codziennej toalecie, ubieraniu
- problemy z utrzymaniem moczu i stolca
- trudności w chodzeniu i staniu
- zmiany zachowania: eskalacja obserwowanych wcześniej i agresja wobec opiekuna
Utrata masy ciała w chorobie Alzheimera
U Twojego podopiecznego może nastąpić utrata masy ciała, ponieważ ten problem dotyka częściej osoby z chorobą Alzheimera niż inne osoby starsze. Chudnięcie możesz zauważyć już w początkowych stadiach choroby Alzheimera, które najczęściej postępuje wraz z jej rozwojem. Dlaczego tak się dzieje? Nie wszystkie przyczyny utraty masy ciała w chorobie Alzheimera są jeszcze znane, ale wśród nich wymienia się:
- pogorszenie funkcjonowania obszarów mózgu regulujących apetyt i zachowania żywieniowe,
- prawdopodobny związek między obecnością genów predysponujących do rozwoju choroby a tendencją do spadku masy ciała,
- obecność białek zapalnych we krwi i mózgu,
- zmiany w funkcjonowaniu układu węchowego.
Jak choroba Alzheimera może wpływać na jakość diety Twojego podopiecznego?
We wczesnych stadiach choroby Alzheimera u Twojego podopiecznego mogą pojawić się problemy z robieniem zakupów, przechowywaniem i przygotowywaniem żywności. Może on także zwyczajne zapominać o tym, czy posiłek został zjedzony czy też nie. Ponadto, przez trudności związane z chorobą, posiłki najczęściej przestają być różnorodne i zbilansowane. Twój podopieczny może zapominać także o regularnym piciu, co znacznie zwiększa ryzyko odwodnienia.
W miarę postępu choroby Twój podopieczny może tracić świadomość co je, co ma zrobić z jedzeniem lub naczyniami postawionymi przed nim. Może odmawiać jedzenia pewnych posiłków lub odmawiać jedzenia w ogóle. Stopniowo może dochodzić także do utraty umiejętności samodzielnego spożywania posiłków. Jedzenie może utrudniać także agresywne i nadpobudliwe zachowanie. Z drugiej strony uspokajające działanie leków będzie zmniejszać dodatkowo apetyt osoby chorej.
U Twojego podopiecznego może rozwinąć się także dysfagia (trudności z połykaniem pokarmów i/lub płynów), która jest zgłaszana u 13-57% chorych.
Ponadto, trudności ze spożywaniem odpowiedniej ilości posiłków u Twojego podopiecznego mogą wynikać także ze zmian w obrębie jamy ustnej, niedostatecznej produkcji śliny czy problemów z uzębieniem i depresji.
Ponieważ postępowi demencji towarzyszy ciągły spadek umiejętności radzenia sobie z czynnościami dnia codziennego takimi jak, np. jedzenie, u Twojego podopiecznego może dojść do niewystarczającego spożycia składników odżywczych. Jednocześnie, choroba i zmiany związane z wiekiem powodują, że zapotrzebowanie na składniki odżywcze rośnie. Tak powstaje błędne koło, które sprawia, że ryzyko rozwoju niedożywienia u Twojego podopiecznego jest bardzo duże.
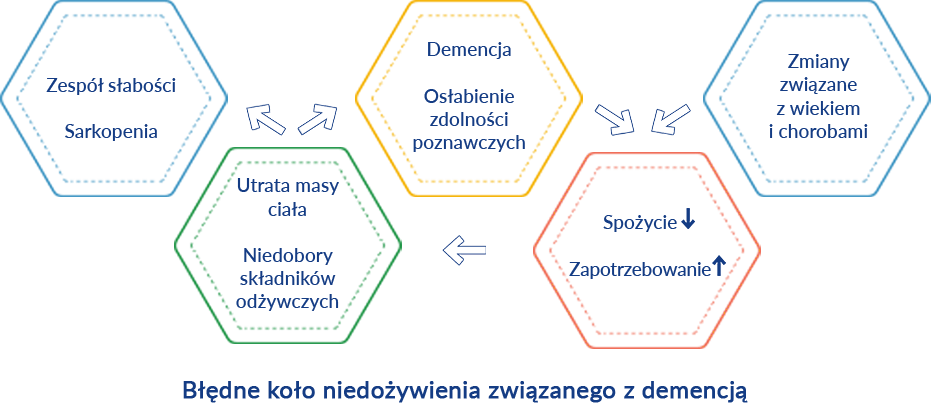
Wsparcie żywieniowe Twojego podopiecznego może przerwać błędne koło i pomóc Wam lepiej radzić sobie z trudami choroby.
Jak zapewnić odpowiednie wsparcie żywieniowe i prawidłową dietę w chorobie Alzheimera?
Przede wszystkim musisz zadbać o jakość podawanych posiłków i kontrolować to, czy są rzeczywiście spożywane. Jeśli samodzielne jedzenie sprawia ogromną trudność, pomóż podopiecznemu w jedzeniu lub nakarm go. Staraj się być cierpliwy i nie okazywać złości i zdenerwowania wobec podopiecznego.
Europejskie Towarzystwo Żywienia Klinicznego i Metabolizmu (ESPEN) rekomenduje podaż osobie chorej na Alzheimera doustnych preparatów odżywczych w celu poprawy stanu odżywienia.14
Ponieważ Twój podopieczny jest w grupie wysokiego ryzyka rozwoju niedożywienia, skonsultuj z lekarzem możliwość wprowadzenia do diety doustnych preparatów odżywczych. Przykładami takich preparatów mogą być Resource 2.0 , Resource 2.0 + Fibre lub Resource Protein . Mają one wygodną, płynną formę, a także występują w różnych smakach, co umożliwia dostosowanie się do upodobań podopiecznego. Wybór doustnego preparatu odżywczego dopasowanego do potrzeb Twojego podopiecznego należy skonsultować z lekarzem, który zdecyduje, czy lepszym rozwiązaniem będzie produkt wysokoenergetyczny, np. Resource 2.0 lub Resource 2.0 + Fibre czy wysokobiałkowy, np. Resource Protein. Lekarz może zasugerować także wzbogacanie klasycznych posiłków w białko przy wykorzystaniu specjalnie stworzonych do tego celu preparatów w proszku, np. Resource Instant Protein.
Polecane produkty
Piśmiennictwo:
- World Alzheimer Report 2009. London, Alzheimer Disease International, 2009. Neurological disorders: public health challenges. Geneva, World Health Organization, 2006
- Swardfager W, Lanctôt K, Rothenburg L, Wong A, Cappell J, Herrmann N (2010). "A meta-analysis of cytokines in Alzheimer disease". Biol Psychiat 68 (10): 930-941
- B. Duthey, Background paper 6.11: Alzheimer disease and other dementias, Priority Medicines for Europe and the World. "A public Health Approach to Innovation", 2004, pp. 1–74.
- Belmin J. Practical guidelines for the diagnosis and management of weight loss in Alzheimer's disease: a consensus from appropriateness ratings of a large expert panel. J Nutr Health Aging 2007;11:33e7.
- Gillette Guyonnet S, Abellan Van Kan G, Alix E, Andrieu S, Belmin J, Berrut G, et al. IANA (International Academy on Nutrition and Aging) Expert Group: weight loss and Alzheimer's disease. J Nutr Health Aging 2007;11:38e48.
- Grundman M, Corey-Bloom J, Jernigan T, Archibald S, Thal LJ. Low body weight in Alzheimer's disease is associated with mesial temporal cortex atrophy. Neurology 1996;46:1585e91.
- Vanhanen M, Kivipelto M, Koivisto K, Kuusisto J, Mykkanen L, Helkala EL, et al. APOE- 4 is associated with weight loss in women with AD: a population- based study. Neurology 2001;56:655e9.
- Zuliani G, Ranzini M, Guerra G, Rossi L, Munari MR, Zurlo A, et al. Plasma cytokines profile in older subjects with late onset Alzheimer's disease or vascular dementia. J Psychiatr Res 2007;41:686e93.
- Stanciu I, Larsson M, Nordin S, Adolfsson R, Nilsson LG, Olofsson JK. Olfactory impairment and subjective olfactory complaints independently predict conversion to dementia: a longitudinal, population-based study. J Int Neuropsychol Soc 2014;20:209e17.
- Lechowski L, de Stampa M, Denis B, Tortrat D, Chassagne P, Robert P, et al. Patterns of loss of abilities in instrumental activities of daily living in Alzheimer's disease: the REAL cohort study. Dement Geriatr Cogn Disord 2008;25:46e53.
- Silva P, Kergoat MJ, Shatenstein B. Challenges in managing the diet of older adults with early-stage Alzheimer dementia: a caregiver perspective. J Nutr Health Aging 2013;17:142e7.
- Chang CC, Roberts BL. Feeding difficulty in older adults with dementia. J Clin Nurs 2008;17:2266e74.
- Alagiakrishnan K, Bhanji RA, Kurian M. Evaluation and management of oropharyngeal dysphagia in different types of dementia: a systematic review. Arch Gerontol Geriatr 2013;56:1e9.
- Volkert D, et al., ESPEN guidelines on nutrition in dementia, Clinical Nutrition (2015), http://dx.doi.org/10.1016/j.clnu.2015.09.004
Żywność specjalnego przeznaczenia medycznego. Stosować pod kontrolą lekarza. Resource 2.0, Resource 2.0+Fibre: Do postępowania dietetycznego w stanach niedożywienia i/lub w przypadku ryzyka niedożywienia. Resource Protein: Do postępowania dietetycznego w stanach niedożywienia i/lub w przypadku ryzyka niedożywienia, któremu może towarzyszyć zwiększone zapotrzebowanie na białko.








